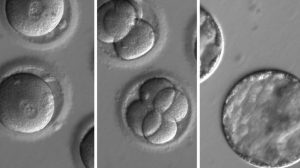
 La scoperta scientifica che ha sorpreso e diviso l’opinione pubblica era trapelata già da qualche giorno, ci ha pensato la rivista scientifica Nature a pubblicare per intero lo studio sugli embrioni umani modificati geneticamente. L’esperimento, avvenuto negli Stati Uniti e coordinato dall’Oregon Health and Science University, ha impiegato la nuova e potentissima tecnica Crispr-Cas9 per correggere un gene responsabile di una malattia cardiaca. Lo sviluppo degli embrioni è stato bloccato dopo pochi giorni: le questioni etiche di fronte all’eventuale nascita di bambini Ogm sono troppo scottanti. Ma se la gravidanza fosse stata portata a termine, non solo sarebbero nati dei bambini sani. Anche i loro figli sarebbero stati al riparo dalla mutazione genetica pericolosa.
La scoperta scientifica che ha sorpreso e diviso l’opinione pubblica era trapelata già da qualche giorno, ci ha pensato la rivista scientifica Nature a pubblicare per intero lo studio sugli embrioni umani modificati geneticamente. L’esperimento, avvenuto negli Stati Uniti e coordinato dall’Oregon Health and Science University, ha impiegato la nuova e potentissima tecnica Crispr-Cas9 per correggere un gene responsabile di una malattia cardiaca. Lo sviluppo degli embrioni è stato bloccato dopo pochi giorni: le questioni etiche di fronte all’eventuale nascita di bambini Ogm sono troppo scottanti. Ma se la gravidanza fosse stata portata a termine, non solo sarebbero nati dei bambini sani. Anche i loro figli sarebbero stati al riparo dalla mutazione genetica pericolosa.
Il gene corretto è responsabile della cardiomiopatia ipertrofica, che colpisce una persona su 500 e può causare tra l’altro la morte improvvisa degli atleti. Si trova sul cromosoma 11. Al momento della fecondazione in vitro, insieme agli spermatozoi portatori del gene malato, i ricercatori hanno introdotto anche Crispr, un sistema composto da due elementi: un enzima capace di tagliare il Dna come un vero e proprio paio di forbici e una sequenza di “lettere” genetiche “scritte” dai ricercatori in laboratorio per indicare il punto esatto in cui tagliare.
Finora due esperimenti simili sugli embrioni umani erano stati condotti in Cina nel 2015 e 2016. In entrambi i casi i risultati erano stati modesti, con molti tagli causati da Crispr in punti sbagliati del Dna. “Noi abbiamo usato una procedura sicura e abbiamo ottenuto un buon grado di efficienza” ha dichiarato oggi Juan Carlos Izpisua Belmonte del Salk Institute, uno dei coautori dello studio. Normalmente, le probabilità di un bambino di ereditare una copia del gene malato da uno dei genitori sarebbero state del 50%. L’intervento di Crispr ha portato questa percentuale al 72% (42 embrioni sui 58 usati), segno che la tecnica di “taglia e incolla del Dna” ha ancora dei tassi di insuccesso rilevanti. “Ma contiamo di poter arrivare al 90, se non al 100%” ha spiegato Shoukrat Mitalipov dell’università dell’Oregon, il coordinatore dello studio.
In compenso, i ricercatori americani (all’esperimento hanno collaborato anche dei genetisti cinesi e sudcoreani) non hanno individuato nessun “danno collaterale” al genoma dei loro embrioni. A volte infatti Crispr – tecnica ancora nuova e controversa, arrivata nei laboratori nel 2012, attorno alla quale è in corso una furiosa battaglia legale per il brevetto – taglia la doppia elica anche in punti diversi rispetto a quello voluto dai ricercatori. Questa è una delle maggiori ragioni di cautela di fronte alla sua applicazione su vasta scala, insieme alla paura che un metodo così semplice ed economico porti alla creazione di “bebè su misura” da parte di laboratori improvvisati.
Le malattie note che sono causate da un singolo gene mutato sono circa 10mila. Teoricamente, potrebbero tutte essere corrette usando Crispr, anche se fra i dettagli dell’esperimento pubblicati oggi da Nature emerge un aspetto che raffredda l’entusiasmo. Quando Crispr taglia il Dna laddove c’è un difetto, la doppia elica tenta subito di ricucirsi. I ricercatori usano allora lo stratagemma di inserire nel nucleo della cellula un gene corretto, che – almeno teoricamente – dovrebbe essere acciuffato dal Dna e usato come toppa. In questo modo è possibile non solo tagliar via un gene mutato, ma anche sostituirlo con una copia artificiale del gene corretto. Nell’esperimento americano questo è avvenuto in un solo embrione: tutti gli altri, fra i 42 in cui Crispr ha agito con successo, avevano semplicemente fatto ricorso alla copia materna del gene, sana in origine. Nelle malattie genetiche in cui anche una sola copia difettosa può provocare problemi, questo tipo di intervento sarebbe stato inutile.
Undici società scientifiche internazionali, tra cui l’American Society of Human Genetics e il Wellcome Trust britannico, hanno già fatto sentire la loro voce di protesta, con una nota che incoraggia gli studi sulle applicazioni cliniche di Crispr, ma chiede anche maggiori cautele (in particolare il divieto di portare avanti gravidanze) nell’uso di una tecnica capace di alterare non solo il Dna di un bambino che ancora dovrà nascere, ma anche quello di tutta la sua discendenza. Di fronte a queste perplessità, Darren Griffin dell’università del Kent lancia però anche un’altra provocazione: “E’ giusto moralmente non intervenire quando abbiamo i mezzi per prevenire una malattia mortale?”.












